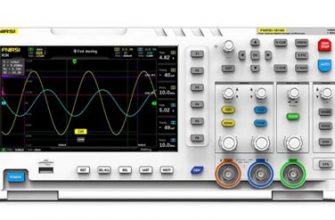
В ходе экспериментальных исследований многие ученые сталкиваются с необходимостью определения количества вещества в указанных образцах. Это важный шаг для достижения точных и надежных результатов и служит базой для дальнейших рассуждений в разных областях науки. Как же определить массу моли вещества? В нашем подробном обзоре мы рассмотрим этот процесс во всех его аспектах, предоставляя полезные советы и подсказки.
Понимание основных понятий:
Прежде чем мы погрузимся в мир определения массово-мольной концентрации вещества, важно уяснить некоторые основные термины, которые помогут нам легче разобраться в этом процессе. Моль – это единица измерения количества вещества и представляет собой количество атомов, молекул или ионов вещества, равное числу атомов в углеродном изотопе-12, составляющем 12 г. Масса – это физическая величина, которая определяет количество вещества, измеренного в граммах. Чтобы определить массу моли, мы должны установить соотношение между масштабами вещества и его количеством.
Способы определения массы моли:
Существует несколько методов, которые позволяют определить массу моли вещества. Один из таких методов – использование химических формул и массовых долей элементов в соединении. Другим способом является расчет на основе известной массы вещества и его массовой доли в образце. Важно понимать, что каждый метод требует определенных данных и рассчитывает массу моли по-разному. В нашем подробном руководстве мы рассмотрим каждый из них в деталях и предоставим примеры для наглядности.
Значение определения количества вещества по массе
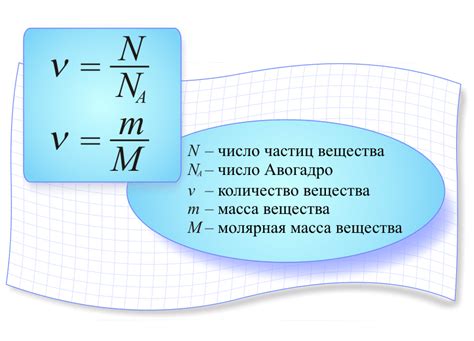
В данном разделе мы рассмотрим важность определения количества вещества при изучении физических и химических процессов. Понимание массы моли вещества помогает нам анализировать и прогнозировать реакции, проводить точные расчеты и достигать результатов, необходимых для достижения конкретных целей.
Значение массы моли
Масса моли вещества, также известная как молярная масса, представляет собой важную физическую величину, которая позволяет нам учитывать массовые соотношения атомов и молекул в химической системе. Определение массы моли является ключевым шагом в решении различных задач, таких как определение состава смесей, расчет объемов газов или прогнозирование образования отдельных химических соединений.
Определение состава вещества
Определение массы моли вещества позволяет нам точно определить его состав и соотношение компонентов. Зная массу моли каждого из элементов или соединений, мы можем составить балансовое уравнение и рассчитать количество реагентов, необходимых для проведения химической реакции. Это позволяет предсказать результаты реакции и контролировать процесс получения определенного продукта.
Например, определение массы моли вещества может быть использовано для расчета объема раствора, содержащего определенное количество растворенного вещества. Это важно для оценки эффективности фармацевтических препаратов или контроля концентрации веществ в промышленных процессах.
Расчеты и изучение реакций
Масса моли вещества играет важную роль во многих расчетах, связанных с химическими реакциями. Зная массу моли реагентов и продуктов реакции, мы можем определить их количественное соотношение и провести расчеты, касающиеся энергетических потребностей, эффективности реакции и прогнозирования ее хода.
Например, зная массу моли вещества, мы можем рассчитать тепловой эффект реакции, которая является важным фактором при изучении реакций горения или синтеза соединений.
Таким образом, определение массы моли вещества позволяет нам получать более точные результаты, проводить анализ физических и химических процессов и прогнозировать результаты, что существенно облегчает наше понимание и контроль над различными системами.
Связь массы моли с химическими расчетами

Определение количества вещества: исчисление числом частиц
В данном разделе рассмотрим метод определения количества вещества путем измерения исчисленым числом частиц, взаимодействующих с данным веществом. Этот подход основывается на принципе статистической механики, где количество вещества выражается величиной, называемой молью.
Изучая свойства атомов, молекул и ионов, можно определить их массу в атомных единицах. Используя эти значения, можно перейти к определению массы моли вещества. Для этого применяется число Авогадро, которое указывает на количество основных частиц в одной моли вещества.
Определение массы моли выполняется путем установления соотношения между массой и количеством частиц. Для этого используется таблица, где против каждого элемента указана его атомная масса. С помощью данных таблицы и числа Авогадро можно просчитать массу одной моли вещества.
| Элемент | Атомная масса (в атомных единицах) |
|---|---|
| Водород | 1.008 |
| Кислород | 16.000 |
| Углерод | 12.011 |
| Азот | 14.007 |
| ... | ... |
Суммируя массы всех атомов, входящих в состав молекулы или иона, и умножая эту сумму на число Авогадро, можно определить массу одной моли данного вещества. Это значительно упрощает расчеты в химических реакциях и позволяет сравнивать различные вещества на основе их мольных характеристик.
Роль определения молекулярной массы: ключ к пониманию химической структуры вещества

Молекулярная масса представляет собой числовое значение, выраженное в единицах атомной массы. Это позволяет исследователям анализировать химические реакции, понимать структуру веществ и предсказывать их свойства. Обладая знанием молекулярной массы, химики могут проводить точные расчеты, основанные на законах химии.
- Определение молекулярной массы помогает определить состав и структуру химических соединений. Измерение молекулярной массы вещества позволяет установить, из каких атомов состоит молекула и в каком количестве.
- Знание молекулярной массы является необходимым условием для расчета реакций, проведения лабораторных исследований и разработки новых химических веществ.
- Определение молекулярной массы помогает устанавливать связи между различными веществами и предсказывать их химические и физические свойства, что является основой для развития новых материалов и промышленных процессов.
- Кроме того, молекулярная масса важна в области анализа веществ, так как позволяет идентифицировать неизвестные соединения и определять их концентрацию.
Таким образом, понимание молекулярной массы и ее роль в химии являются ключевыми для достижения прогресса в различных областях науки и технологии. Использование точных методов определения молекулярной массы позволяет находить новые решения и совершенствовать существующие процессы, что способствует развитию нашего мира.
Разнообразные способы расчета количество материи
Этот раздел посвящен обсуждению различных методов, которые позволяют определить количество вещества в образце. Здесь мы рассмотрим разнообразные подходы и подчеркнем их важность в химическом анализе.
1. Стоимость вещества: Иногда можно приблизительно определить количество вещества, основываясь на стоимости образца. Вещества с высокой ценой обычно содержат в себе меньшее количество молей, в то время как более дешевые вещества могут быть доступны в больших количествах.
2. Объем и плотность: Еще один метод основывается на измерении объема и плотности вещества. Зная объем образца и его плотность, можно рассчитать массу и, следовательно, количество молей вещества.
3. Молярная масса: Молярная масса - это масса одной моли вещества. Путем измерения массы образца и зная его молярную массу, можно расчитать количество молей вещества.
4. Реакционные соотношения: Химический анализ основан на реакционных соотношениях между различными веществами. Используя заранее известные соотношения, можно рассчитать количество молей вещества.
5. Газовые законы: В некоторых случаях, при работе с газами, можно применять газовые законы для определения количества молей вещества. Такие законы, как закон Гей-Люссака или закон Бойля-Мариотта, предоставляют информацию о количестве молей газа.
Важно понимать, что разные методы могут быть применимы в разных ситуациях и с разными типами веществ. Также необходимо учитывать возможность ошибок и неточностей при использовании этих методов. Но сочетание различных подходов и аккуратность при расчетах позволяют достичь более точных результатов.
Вопрос-ответ

Как определить массу моли вещества?
Определение массы моли вещества осуществляется путем деления массы данного вещества на его молярную массу. Молярная масса — это масса одного моля вещества, выраженная в граммах. Для подсчета молярной массы необходимо умножить атомную массу каждого элемента в веществе на его количество атомов, указанное в химической формуле.
Как правильно измерить массу вещества?
Для измерения массы вещества необходимо использовать весы или аналитические взвешивающие приборы. Взвесьте пустой контейнер, а затем добавьте нужное количество вещества в контейнер и снова проведите взвешивание. Вычтите массу пустого контейнера из общей массы, чтобы получить массу вещества.
Какие единицы измерения обычно используются для молей?
Для измерения молей чаще всего используется единица измерения грамм/моль (г/моль). Она обозначает массу одного моля вещества. Однако иногда также могут применяться другие единицы, такие как кг/моль (килограмм/моль) или мг/моль (миллиграмм/моль), в зависимости от масштабов и точности измерений.
Какое значение имеет масса моли в химии?
Масса моли в химии является важным понятием, которое позволяет совместить микроскопическую и макроскопическую точки зрения на вещество. Масса моли позволяет химикам проводить расчеты, определять количество вещества и осуществлять конверсии между массой и количеством вещества, что является фундаментальным в химических реакциях и определении состава различных соединений.