В химии существует немало методов для вычисления основной характеристики вещества - молярной массы. Это значимый параметр, отвечающий за массу одного моля вещества. Физические и химические свойства вещества тесно связаны с его молярной массой.
Представьте себе, что вы химик и вам необходимо определить молярную массу неизвестного вещества. Это может показаться сложным на первый взгляд, но на самом деле, есть несколько способов получить этот результат без нужды в специальных аппаратах и сложных формулах.
Один из способов - использование изменения температуры при смешении различных веществ. Другой метод основан на способности вещества взаимодействовать с электромагнитным полем. Также, существуют методы, которые основаны на реакциях веществ с кислородом, водой и другими реагентами.
Изначальное понятие массы в научной области, изучающей соединения веществ, а также процессы, протекающие между ними
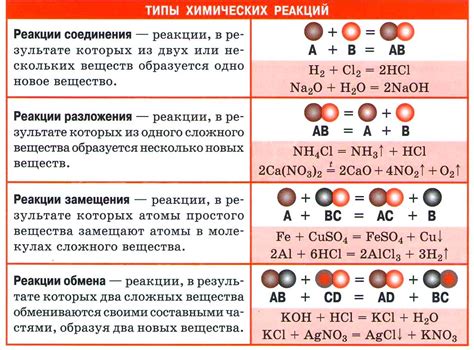
Молярная масса в химии обозначает сравнительную массу вещества относительно атомной массовой единицы. Она измеряется в граммах на моль и является суммой масс атомов всех элементов, составляющих молекулу вещества. Понятие молярной массы было введено для облегчения расчетов и анализа соединений в химических реакциях.
- Важность понятия молярной массы
- Изучение и определение массы вещества
- Роль молярной массы в химических расчетах
- Влияние молярной массы на свойства вещества
- Исторический аспект понятия молярной массы
Знание о молярной массе вещества позволяет ученым предсказывать и объяснять его физико-химические свойства и взаимодействия с другими веществами. Осознание истории и эволюции этого понятия помогает студентам и ученым более глубоко понять его суть и применение в реальных химических задачах.
Основа и назначение понятия атомной массы в химии

В химии, существует важное понятие, которое играет решающую роль в многих аспектах изучения вещества. Это понятие, которое положило основу для понимания состава и структуры вещества, называется... понятие атомной массы, оно также может называться молекулярной массой, бруттоформулой или атомарным весом. Важно отметить, что назначение этого понятия заключается в определении количества вещества, а также в определении его свойств и реакционных способностей.
| Атомная масса: | Величина, определяющая массу одного атома элемента или молекулы соединения. Обычно выражается в атомных единицах (у). Меньший элемент в атомной таблице Менделеева также называется ядром атомной элемента, в то время как более сложная структура из атомов называется молекулой. |
| Молекулярная масса: | Сумма атомных масс всех атомов в молекуле. Она выражается в массовых единицах, таких как граммы на моль (г/моль) или килограммы на моль (кг/моль). |
| Бруттоформула: | Это формула, которая указывает количество и атомный состав каждого элемента в соединении. |
| Атомарный вес: | Термин, используемый вместо атомной массы для указания массы одного атома или молекулы. |
Понимание и использование понятия атомной массы является ключевым для проведения расчетов в химии. Он позволяет нам определить количество молекул или атомов вещества, а также вычислить массу вещества в определенном количестве. Например, зная молекулярную массу вещества, мы можем определить, сколько граммов этого вещества содержится в одной молекуле или в одной моли. Это необходимо для проведения экспериментов, синтеза новых веществ и понимания их химических свойств и реакционных способностей.
Методы определения массы вещества при исследованиях в химической науке

Этот раздел посвящен различным подходам и инструментам, используемым химиками для определения массы вещества в рамках своих исследований. Методы, которые приведены ниже, помогают установить точную мольную массу материала и определить его состав.
Один из основных методов, применяемых при определении массы вещества, - это гравиметрический анализ. Он основан на измерении массы вещества и рациональном использовании законов химии для получения результатов. Качественные и количественные анализы могут быть выполнены с использованием этого метода, позволяющего определить точную массу и состав вещества.
Другим распространенным методом является волюметрический анализ, который основан на измерении объема растворов и концентрации вещества. В этом методе химики используют титрование, чтобы определить точную массу вещества. Титрование позволяет измерить количество реагента, необходимого для реакции с изучаемым веществом и определить его массу.
Также существуют инструменты и техники, основанные на спектрофотометрии, масс-спектрометрии и электрохимическом анализе, которые предоставляют дополнительные возможности для измерения мольной массы и состава вещества. Эти методы позволяют определить массу и концентрацию вещества на основе измерений света, массы его заряженных частиц или электрической активности вещества.
Все эти методы являются неотъемлемой частью химических исследований и обеспечивают точные и надежные результаты для определения мольной массы вещества, что является важным вкладом в развитие химии и научных открытий в этой области.
Описание различных путей расчёта массы одного моля вещества в области химических исследований

В химии существует несколько методов определения массы одного моля вещества, которые играют ключевую роль в различных химических исследованиях. Эти методы обеспечивают возможность вычисления молекулярных масс разных соединений и применения полученных данных в различных областях, включая синтез новых веществ, изучение ионных реакций и определение состава образцов.
Один из подходов к определению массы одного моля основывается на измерении массы определенного объема (например, 22.4 литра) газа при стандартных условиях температуры и давления. Такой метод, известный как метод газовых молей (или метод Авогадро), основан на предположении, что при стандартных условиях все идеальные газы содержат одинаковое количество молей в одном и том же объеме. Зная массу газа, можно рассчитать массу одного моля этого газа.
Второй метод, известный как метод относительных атомных масс, основывается на рассмотрении состава вещества из его атомов и молекул. Для этого метода необходимо знать массу атомов и молекул различных элементов, а также их количества в соединении. С помощью этой информации можно определить суммарную массу всех атомов или молекул вещества и затем выразить ее в граммах. Зная массу одного моля вещества, можно рассчитать массу одной молекулы или атома.
Третий метод, называемый методом коллективной массы, основывается на анализе результата химической реакции. Расчет производится на основе знания пропорций вещества в реакции и изменения массы вещества до и после реакции. Этот метод учитывает сохранение массы вещества и позволяет определить массу одного моля вещества на основе известных данных о массе других веществ, участвующих в реакции.
| Метод | Описание |
|---|---|
| Метод газовых молей | Основан на измерении массы газа при стандартных условиях температуры и давления |
| Метод относительных атомных масс | Основан на рассмотрении состава вещества из его атомов и молекул |
| Метод коллективной массы | Основан на анализе результата химической реакции и изменении массы вещества |
Расчет молярной массы на основе информации о химической формуле

Первым шагом при расчете молярной массы по химической формуле является определение атомного состава вещества. Для этого необходимо подсчитать количество атомов каждого элемента, присутствующего в формуле. Это можно сделать путем анализа и разбора формулы на составляющие элементы.
После определения атомного состава, следует установить относительные атомные массы для каждого элемента. Они указываются в периодической системе химических элементов и обозначаются числовыми значениями. Для расчета молярной массы необходимо умножить количество атомов каждого элемента на его относительную атомную массу.
Далее, полученные значения следует суммировать, чтобы получить общую молярную массу вещества. Это позволит определить массу одного моля вещества, которая выражается в граммах и является основой для дальнейших расчетов.
Расчет молярной массы по данным химической формулы является важным инструментом для химиков при проведении различных теоретических и практических исследований. Он позволяет установить соотношение массы вещества и числа его атомов, что необходимо для понимания и манипулирования химическими реакциями и процессами.
Путь к определению величины, обозначающей суммарную массу вещества

Нет сомнений, что в практической химии каждый химик сталкивается с необходимостью вычисления численного значения, которое представляет собой суммарную массу вещества. Понимание процесса вычисления молярной массы имеет фундаментальное значение для понимания химических реакций и взаимодействий.
Когда мы говорим о молярной массе, мы обозначаем величину, которая определяет массу одного моля вещества. Важно понимать, что молярная масса может быть выражена в различных единицах измерения, таких как грамм, килограмм или атомная единица массы. Математически молярная масса вычисляется путем сложения масс всех атомов или молекул, образующих вещество.
Процесс вычисления молярной массы можно наглядно пояснить на примере простого вещества, такого как вода (H2O). Возьмем во внимание, что вода состоит из двух атомов водорода (H) и одного атома кислорода (O). Массы атомов водорода и кислорода, обозначенные как mH и mO соответственно, могут быть найдены в химических таблицах элементов. Далее, необходимо умножить массу каждого атома на количество атомов в молекуле воды. Например, если mH = 1 г/моль и mO = 16 г/моль, то молярная масса воды будет равна (2 * 1 г/моль) + (1 * 16 г/моль) = 18 г/моль.
Определение молярной массы через экспериментальные методы

Первым методом, который будет рассмотрен, является метод определения молярной массы через измерение давления паров вещества. В этом методе используется уравнение Клапейрона-Клаузиуса, которое связывает давление, объем, температуру и количество вещества. Путем измерения давления паров при разных температурах можно получить данные, необходимые для определения молярной массы.
- Измерение давления паров вещества
- Определение температурных изменений
- Расчет молярной массы с использованием уравнения Клапейрона-Клаузиуса
Второй метод, называемый методом количественного анализа, основан на химических реакциях и использовании стехиометрических соотношений между веществами. Путем проведения определенных реакций, измерения количества реагентов и продуктов реакции можно получить данные для вычисления молярной массы.
- Выбор химической реакции с известными стехиометрическими соотношениями
- Измерение количества реагентов и продуктов реакции
- Расчет молярной массы с использованием стехиометрических соотношений и закона сохранения массы
Третий метод, который будет рассмотрен, основан на использовании коллоидных растворов и определении их коллоидной стабильности. Коллоидные растворы представляют собой систему, в которой дисперсная фаза находится в состоянии постоянного равновесия с диспергирующей средой. Путем измерения определенных параметров коллоидной системы можно получить данные для расчета молярной массы.
- Выбор коллоидной системы с известной молярной массой
- Измерение параметров коллоидной системы, связанных с коллоидной стабильностью
- Расчет молярной массы путем анализа полученных данных
Таким образом, использование экспериментальных методов позволяет определить молярную массу вещества, являющуюся важным параметром в химических расчетах и исследованиях.
Вопрос-ответ

Какие существуют способы вычисления молярной массы в химии?
В химии существует несколько способов вычисления молярной массы вещества. Один из основных способов - это сумма атомных масс всех атомов, входящих в молекулу вещества. Для этого необходимо знать химическую формулу и атомные массы всех элементов. Другой способ - определение молярной массы при помощи экспериментальных данных, таких как плотность и объем вещества. Также можно использовать спектральные методы, такие как масс-спектрометрия, для определения молярной массы.
Можно ли вычислить молярную массу вещества без знания его химической формулы?
Нет, без знания химической формулы невозможно точно вычислить молярную массу вещества. Химическая формула указывает, из каких элементов состоит вещество и в каких соотношениях. Для вычисления молярной массы необходимо знать атомные массы этих элементов. Однако, в некоторых случаях можно примерно оценить молярную массу, если есть данные о составе вещества или его свойствах.
Какими инструментами можно определить молярную массу вещества?
Для определения молярной массы вещества можно использовать различные инструменты. Один из них - это периодическая система химических элементов, где указаны атомные массы всех элементов. С помощью периодической системы можно определить мольные массы отдельных элементов и вычислить молярную массу вещества, суммируя массы всех атомов. Также можно использовать химические калькуляторы онлайн, где можно ввести химическую формулу и получить мольную массу вещества. Для более точных определений молярной массы можно применять спектральные методы, например, масс-спектрометрию.